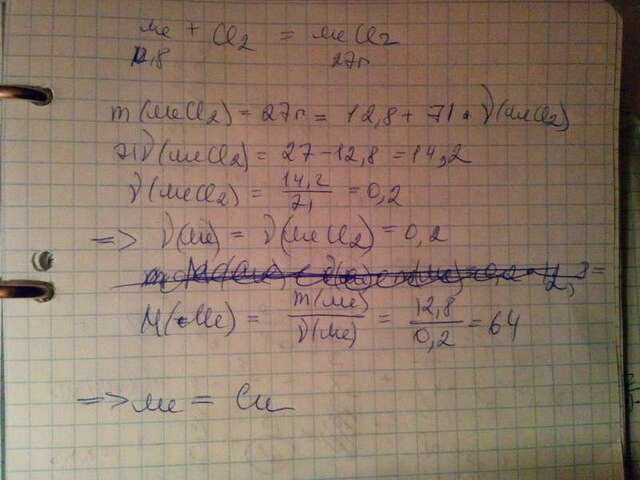В дано, я так понимаю, будет достаточно записать общую реакцию с абстрактным металлом (Ме) и стехеометрическими коэффициентами, массы металла, вступившего в реакцию и образовавшегося хлорида.
Решение:
Очень удобно, что все коэффициенты в уравнении у нас единичные.
По уравнению мы видим, что масса всего металла, вступившего в реакцию переходит в хлорид.
Следовательно, масса хлорида = масса металла + масса хлора, вступившего в реакцию
Поскольку масса вещества равна произведению молекулярной массы и молярной концентрации, мы по этому соотношению легко находим массу металла.
Далее по таблице Менделеева находится наиболее близкий по массе металл.
Которым оказывается медь