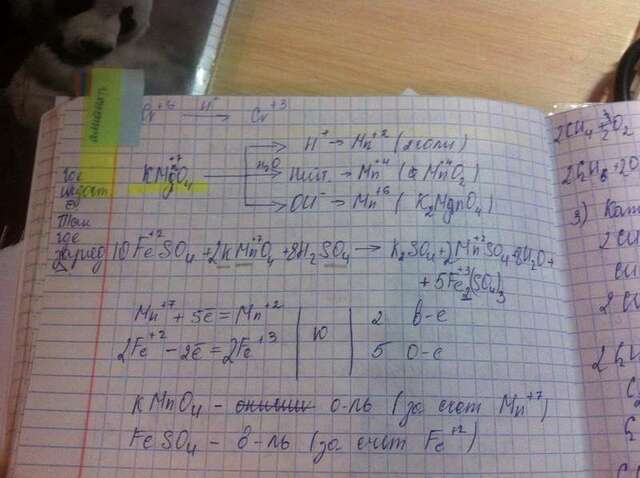Лично мне помогает "вилка", то есть если в реакцию вступает КMnO4, то возможно 3 варианта.
1. если все происходит в Кислой среде, то Mn окисляется до степени +2 (MnCl2) и тут всегда образуются 2 соли)
2. если все происходит в Нейтральной среде (тобишь вода), то Mn окисляется до степени +4 (MnO2)
3. если все происходит в Щелочной среде, то Mn окисляется до степени +6 (K2MnO4)
УДАЧИ))