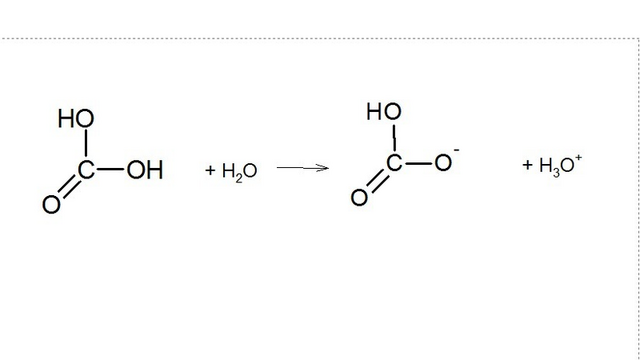
Угольная кислота относится к двухосновным кислотам, поэтому образует два типа солей карбонаты и гидрокарбонаты.
В водном растворе существует равновесная система
СО₂ + Н₂О ⇔ СО₂*Н₂О ⇔ Н₂СО₃
Н₂СО₃ ⇔ Н⁺ + НСО₃⁻ гидрокарбонат-анион
НСО₃⁻ ⇔ Н⁺ + СО₃²⁻ карбонат-анион
CO2 (избыток) + NaOH (раствор) = NaHCO3
в этой реакции сначала образуется карбонат-ион, при избытке углекислого газа переходящий в гидрокарбонат
Na2CO3+CO2+H2O=2NaHCO3
СО₃²⁻ + Н₂О ⇔ НСО₃⁻ + ОН⁻ гидролиз карбонат-аниона