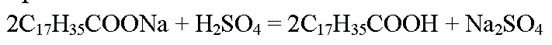Дано:
m (мыла) = 250 г
w(C17 H35COONa) = 68%
w выхода – 92 %
Найти:
m (C17H35COOH) -?
Решение:
170 г х
г
306*2 284*2
1. Найдем массу стеарата натрия:
m(C17 H35COONa) = 250×0,68= 170 г
М(C17 H35COONa) = 306 г/моль
М(C17H35COOH) = 284 г/моль
2. Чтобы найти массу стеариновой кислоты, составим пропорцию
170*284*2 = х*306*2
х = 96560/612 = 157, 78 г
5. Найдем массу m(C17H35COOH) с выходом кислоты 92%:
157,78×0,92 = 145,16 г
Ответ: 145,16 г