1) S --> P ---> Al --> Mg
металлические св-ва увеличиваются в периодах справа налево, так уменьшается число внешних электронов и атом их легче отдает
2) ²⁴Mg(12,12e,12n)
на внешнем уровне - 2е
число электронных слоёв - 3
¹²C(6p,6e,6n)
на внешнем уровне - 4е
число электронных слоёв - 2
³²S(16p, 16e, 16n)
на внешнем уровне - 6е
число электронных слоёв - 3
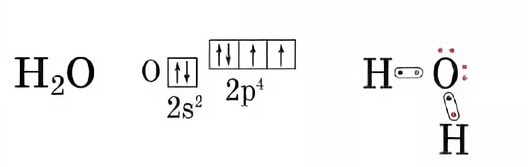
3) ковалентно-полярная связь: H2O, SО3
Fe2О3(ионная), NaCl(ионная) CaO(ионная), ,Н2(ковалентно-неполярная)
схема в фото
4) Ar(Si) = 28
IV группа, главная подгруппа, 3 малый период. 3 ряд
+14 ) ) )
2 8 4
1s² 2s² 2p⁶ 3s² 3p² -электронная формула
5)
Mr(Fe₂O₃) = 56*2+16*3 = 160
w(O) = Ar(O)*n(O)\Mr(Fe₂O₃) = 16*3\160 = 0,3 , или 30%