Химические свойства:
1. галогенирование
CH2=CH2+Br2 = CH2Br-CH2Br
2. гидрогалогенирование
CH2=CH2 +HCl = CH3-CH2Cl
3. горения
CH2=CH2 + 3O2 = 2CO2 + 2H2O (нагревание)
4. Окисление
- мягкое
3CH2=CH2 + 4H2O + 2KMnO4 = 2MnO2 + 2KOH + CH2(OH)-CH2(OH)
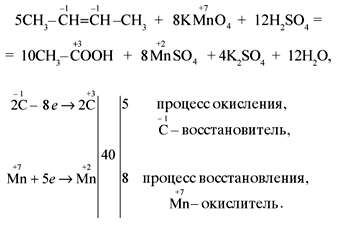
-жесткое
(смотреть фото)
5. Гидратация
CH2=CH2+H2O = CH3-CH2(OH) (обязательно катализатор H2SO4)
6. Гидрирование
CH2=CH2 + H2 = CH3-CH3( катализатор Ni,Pt,Pd ; при нагревании)
7. Дегидрирование
CH2=CH2 = CH=-CH(тройная связь) + H2( катализатор Ni,Pt,Pd ; при нагревании)
8. Полимеризация
nCH2=CH2 = [-CH2-CH2-]n ( n - степень полимеризации )
Физические свойства:
Вступают в реакции присоединения. Активные в-ва, т.к. имеют непрочную Пи-связь. Находятся в sp2-гибридизации ; валентный угол равен 120 градусам ; длина связи = 0,134 нм ; энергия связи больше, чем у алканов, но меньше, чем у алкинов.
В молекуле КПС , а значит МКР(молекулярная кристаллическая решетка), а значит температуры кипения и плавления выше, чем у алканов. Алкены нерастворимы в воде.