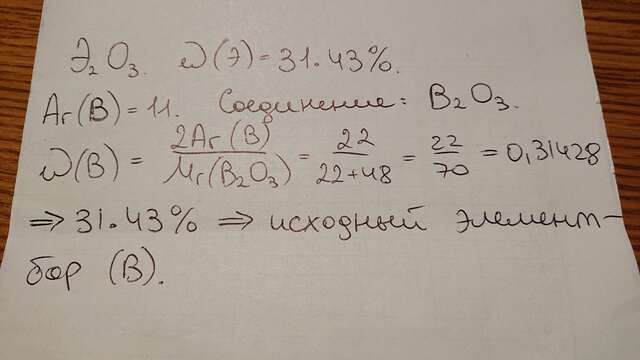1. Оксид элемента 3 группы имеет общий вид Э2О3 (Э - элемент).
Начнём с бора. Его относительная атомная масса 11.
31.43 = 2Ar(B) ÷ (2Ar(B) + 3Ar(O)) =
22 ÷ (22 + 48) = 31.48. Значит, исходный элемент - бор (В).
2. a) Mr(Cu(OH)2) = 64 + 32 + 2 = 98.
б) Mr(K3PO4) = 3×39 + 31 + 64 = 212.
в) Mr(MgCl2) = 24 + 35.5×2 = 95.
г) Mr(Fe2(SO4)3) = 56×2 + 32 + 64 = 208.
3. Весь объём равен 107 литров.
Кислород: 20 ÷ 107 = 19%
Азот: 40 ÷ 107 = 37%
Углекислый газ: 35 ÷ 107 = 33%
Хлор: 12 ÷ 107 = 11%
4. Масса вещества равна 0.15 × 80 = 12 грамм. Значит, его массовая доля в растворе массой (80 + 30) 110 грамм равна 12 ÷ 110 = 11%
5. Масса соли в первом растворе 70 × 0.3 = 21 грамм, во втором - 210 × 0.1 = 21 грамм, значит, вся масса соли равна 42 грамма. Весь раствор имеет массу 280 грамм, следовательно массовая доля соли равна 42 ÷ 280 = 15%.
6. Оксид алюминия - Al2O3
Оксид кремния (4) - SiO2
Оксид железа (3) - Fe2O3
Оксид водорода - Н2О
Оксид углерода (4) - СО2
Оксид углерода (2) - СО
Оксид серы (4) - SO2
Оксид азота (2) - NO
Оксид азота (4) - NO2